

Una vez conocidas las formas y tamańos de los orbitales atómicos, hablaremos ahora de sus energía relativas y cómo estos niveles de energía ayudan a determinar las distribuciones electrónicas reales encontradas en los átomos. De acuerdo a la ecuación:
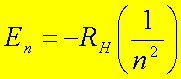 |
... la energía de un electrón en un átomo esta determinada sólo por su número cuántico principal. Así, las energías de los orbitales del hidrógeno aumentan como sigue:
1s<2s=2p<3s=3p=3d<4s=4p=4d=4f<...
A pesar de que la distribución de densidad electrónica es diferente en los orbitales 2s y 2p, los electrones del hidrógeno tienen la misa energía ya sea en los orbitales 2s o 2p. Se dice que los orbitales que tienen la misa energía están degenerados. El orbital 1s en el átomo de hidrógeno corresponde a la máxima estabilidad y se le llama estado fundamental; un electrón que se ubique en este orbital será el más fuertemente atraido por en núcleo. Un electrón en 2s o 2p u otros orbitales superiores en un átomo de hidrógeno estará en un estado exitado.
El diagrama energético es diferente átomo polielectrónico. La energía de un electrón de un átomo polielectrónico, a diferencia del átomo de hidrógeno, depende no solo de su número cuántico principal sino también de su número cuántico azimutal (figura 1). En un átomo polielectrónico, el subnivel 3d está muy cerca del subnivel energético 4s. La energía total del átomo depende no solo de las suma de las energías de los orbitales sino tambien de la energía de repulsión electrónica en estos orbitales. Resulta que la energía total de un átomo es menor cuando se llena la subcapa 4s antes que las 3d. La figura 2 constituye un diagrama de apoyo útil en la selección del orden de llenado de los orbitales atómicos en un átomo polielectrónico.
 |
| Figura 1: Niveles de energía de los orbitales de un átomo de hidrógeno. Cada línea horizontal pequeńa representa un orbital. Todos los orbitales tienen el mismo numero cuantíco principal (n), por lo tanto, tienen la misa energía. |
 |
| Figura 2: Niveles de energía de los orbitales de un átomo polielectrónico. Obserce que la energía del nivel dependende tanto del valor de n como el de l. |